Produknaam:Metieletielketoon
Molekulêre formaat:C4H8O
CAS-nommer:78-93-3
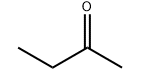
Produk molekulêre struktuur:
Spesifikasie:
| Item | Eenheid | Waarde |
| Suiwerheid | % | 99.8 min |
| Kleur | APHA | 8max |
| Suurwaarde (as asetaatsuur) | % | 0.002maks |
| vog | % | 0.03maks |
| Voorkoms | - | Kleurlose vloeistof |
Chemiese Eienskappe:
Metieletielketoon is vatbaar vir verskeie reaksies as gevolg van sy karbonielgroep en die aktiewe waterstof langs die karbonielgroep. Kondensasie vind plaas wanneer dit met soutsuur of natriumhidroksied verhit word om 3,4-dimetiel-3-hekseen-2-oon of 3-metiel-3-hepteen-5-oon te produseer. Wanneer dit vir 'n lang tyd aan sonlig blootgestel word, word etaan, asynsuur en kondensasieprodukte geproduseer. Genereer diasetiel wanneer dit met salpetersuur geoksideer word. Wanneer dit met sterk oksideermiddels soos chroomsuur geoksideer word, word asynsuur gegenereer. Butanoon is relatief stabiel teen hitte, en termiese splitsing by hoër temperature produseer enoon of metielenoon. Wanneer dit met alifatiese of aromatiese aldehiede gekondenseer word, word hoë molekulêre gewig ketone, sikliese verbindings, ketoonkondensasie en harse geproduseer. Byvoorbeeld, kondensasie met formaldehied in die teenwoordigheid van natriumhidroksied produseer eers 2-metiel-1-butanol-3-oon, gevolg deur dehidrasie tot metakrilatoon.
Harsvorming vind plaas na blootstelling aan sonlig of UV-lig. Kondensasie met fenol lewer 2,2-bis(4-hidroksifeniel)butaan. Reageer met alifatiese esters in die teenwoordigheid van 'n basiese katalisator om β-diketone te produseer. Asilering met suuranhidried in die teenwoordigheid van 'n suur katalisator om β-diketone te vorm. Reageer met waterstofsianied om sianohidrien te vorm. Reageer met ammoniak om ketopiperidienderivate te vorm. Die α-waterstofatoom van butanoon word maklik met halogene vervang om verskeie gehalogeneerde ketone te vorm, soos 3-chloro-2-butanoon deur interaksie met chloor. Interaksie met 2,4-dinitrofenielhidrasien produseer geel 2,4-dinitrofenielhidrasoon.
Toepassing:
Metieletielketoon (2-butanoon, etielmetielketoon, metielasetoon) is 'n organiese oplosmiddel met relatief lae toksisiteit, wat in baie toepassings voorkom. Dit word in industriële en kommersiële produkte gebruik as 'n oplosmiddel vir kleefmiddels, verf en skoonmaakmiddels, en as 'n ontwasmiddel. Metieletielketoon, 'n natuurlike komponent van sommige voedselsoorte, kan deur vulkane en bosbrande in die omgewing vrygestel word. Dit word gebruik in die vervaardiging van rooklose poeier en kleurlose sintetiese harse, as 'n oplosmiddel en in oppervlakbedekkings. Dit word ook as 'n geurmiddel in voedsel gebruik.
MEK word as 'n oplosmiddel vir verskeie bedekkingstelsels gebruik, byvoorbeeld viniel, kleefmiddels, nitrosellulose en akrielbedekkings. Dit word gebruik in verfverwyderaars, lakke, vernis, spuitverf, seëlaars, gom, magnetiese bande, drukinkt, hars, hars, skoonmaakoplossings en vir polimerisasie. Dit word in ander verbruikersprodukte aangetref, byvoorbeeld huishoudelike en stokperdjiesement en houtvulprodukte. MEK word gebruik in die ontwas van smeerolies, die ontvetten van metale, in die produksie van sintetiese leer, deursigtige papier en aluminiumfoelie, en as 'n chemiese tussenproduk en katalisator. Dit is 'n ekstraksie-oplosmiddel in die verwerking van voedsel en voedselbestanddele. MEK kan ook gebruik word om chirurgiese en tandheelkundige toerusting te steriliseer.
Benewens die vervaardiging daarvan, sluit omgewingsbronne van MEK die uitlaatgasse van straal- en binnebrandenjins, en industriële aktiwiteite soos die vergassing van steenkool in. Dit word in aansienlike hoeveelhede in tabakrook aangetref. MEK word biologies geproduseer en is geïdentifiseer as 'n produk van mikrobiese metabolisme. Dit is ook gevind in plante, insekferomone en dierweefsels, en MEK is waarskynlik 'n klein produk van normale soogdiermetabolisme. Dit is stabiel onder gewone toestande, maar kan peroksiede vorm met langdurige berging; hierdie kan plofbaar wees.
Produkte kategorieë
-

Foon
-

E-pos
-

Whatsapp
-

Bo













